
不溶性微粒应用专题 | ALP_AN_208_CN_医药包材不溶性微粒检查的要求
奥法美嘉微纳米应用工程中心 - 廖军

本文隶属于不溶性微粒应用专题,全文共 3829字,阅读大约需要 12 分钟
《中国药典》2025版正式发布前,医药企业对药包材不溶性微粒的质量控制主要参照2015年版《YBB002722004-2015包装材料不溶性微粒测定法》,重点针对药用胶塞、输液瓶、输液袋及塑料输液容器内盖等产品。2025版药典新增<4206>药包材不溶性微粒测定法,在原有YBB标准的基础上全面进行了升级,构建了“1+4+58”标准体系,以9621通用要求为总纲,配套玻璃、橡胶、塑料、金属四大类材质专项原则及八项检测方法,适用范围从传统玻璃、塑料扩展到金属等更多材质[1][2]。新标准明确规定注射剂包装用橡胶密封件、塑料包装系统及组件、预灌封注射器活塞、笔试注射器活塞、半组装预灌封注射器、笔试注射器用卡式瓶系统、药品包装用金属容器等均需开展不溶性微粒检测,实现对医药包材的全面覆盖。从源头控制微粒的风险,提升药品安全性和有效性。
图1:常见的输液袋、胶塞、预灌封注射器等药包材

<4206>药包材不溶性微粒测定法中规定了检测方法,分别是光阻法和显微计数法,其中光阻法为首选方法。当光阻法结果异常或样品不适用时,显微计数法作为补充,通过两者双重质控,保障测试数据的可靠性。
实验环境和仪器校准:照《中国药典》2025版四部通则0903下规定进行[3]。
光阻法检查用水要求:取 5 份检查,每份 5mL,25mL 中含 10μm 及 10μm 以上的不溶性微粒数应在 25 粒以下,含 25μm 及 25μm 以上的不溶性微粒数应在 5 粒以下。
光阻法仪器校准周期:仪器应定期校准,至少每年校准一次。
体积准确性:连续测定3次,每次测得体积与量取积的示值之差应在±5%以内。测得体积的平均值与量取体积的示值之差应在土3%以内 ;
计数准确性:取平均粒径为10μm的标准粒子,依法测定3次,记录5μm通道的累计计数,弃第一次测定数据,后两次测定数据的平均值与已知粒子数之差应在20%以内;
传感器分辨率:取平均粒径为10μm的标准粒子,依法测定8μm、10μm、12μm三个通道的粒子数,计算8μm 10μm两个通道的差值计数和10μm与12μm两个通道的差值计数,上述两个差值计数与10μm道的累计计数之比都不得小于68%。
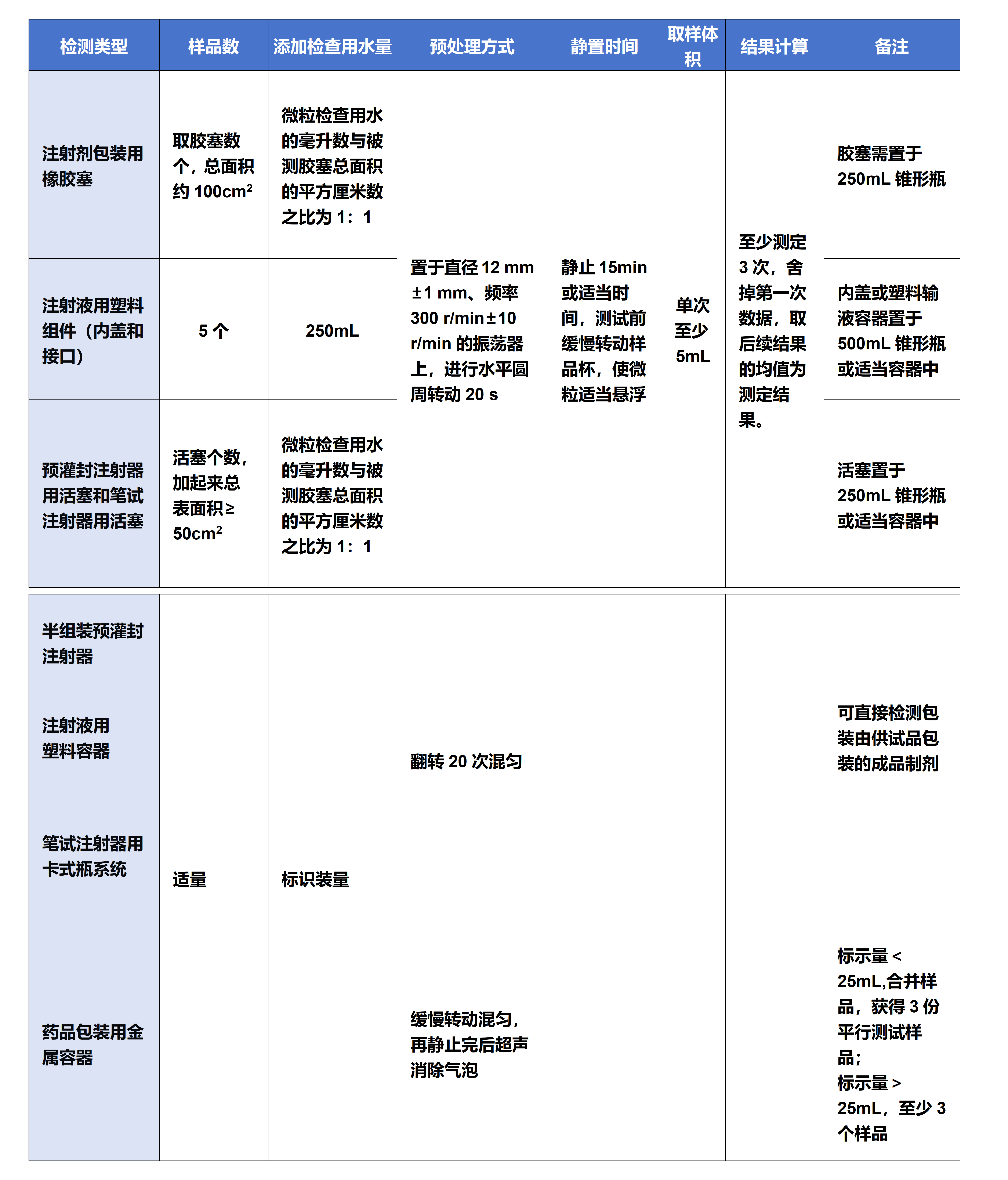
表1供试品的制备工作及检测要求[4]
虽然《中国药典》2025版<4206>章节未直接给出药包材不溶性微粒的判定限值,但药典委在官方解读中“2025版《中国药典》颁布后,药包材标如何执行”,对此进行了回复:药包材企业应在确认包材符合预期药用要求的基础上,遵照关联审评的相关规定,并参考2025版《中国药典》药包材相关指导原则及2015版YBB品种标准,确定质量标准,进行质量控制[5]。因此,不溶性微粒的判定结果仍可沿用YBB标准中的限度,确保质量控制有据可依,详细判断限制见表2。
表2 2015 版 YBB 标准对药品包装材料与容器的不溶性微粒限度要求:

图2:静脉注射过程示意图

根据2025版《中国药典》<4206>药包材不溶性微粒测定法要求,需对注射剂用橡胶密封件、塑料容器、预灌封注射器活塞及金属容器等关键组件进行不溶性微粒检测。试验时,注入检查用水至容器或清洗活塞表面得到脱洗液,其体积范围从15mL至250mL不等。对于体积较少的脱洗液,使用标准配置的不溶性微粒分析仪Accusizer® A2000USP,每次抽取5mL样品,连续3次抽取即可完成检测。而体积较大的脱洗液(如250mL或更多),若仍按5mL体积取样,计算时需舍去首次数据,取后续几次检测结果均值。然而,实际操作中发现,几次检测结果可能呈现重复性较差且均值超标的情况。操作人员常将此归咎于仪器稳定性问题。但实际情况是抽样体积过少,对包材测试结果的影响尤为显著。较小的样品量往往无法充分代表包材的整体特性,导致测试数据出现偏差或不准确,进而影响结果的可靠性和重现性。
针对这一挑战,我们推荐采用蠕动泵抽样的不溶性微粒分析仪Accusizer® A2000USP。该设备能够实现一整瓶(袋)样品的连续抽样检测,有效避免了因检测体积过小而导致的测试结果不准确问题。通过增大抽样量,配备蠕动泵抽样功能的Accusizer® A2000USP可以更全面地捕捉包材中的细微特征,显著提升测试数据的代表性和准确性。这不仅有助于解决当前面临的重复性差和均值超标问题,还能为包材质量评估提供更为可靠的科学依据。

图3:采用蠕动泵抽样的不溶性微粒分析仪Accusizer® A2000USP

AccuSizer® A2000系列采用单颗粒光学传感计数(Single Particle Optical Sizing,SPOS)技术,可以为注射剂和医药包材的不溶性微粒检提供安全、快捷、高效、可靠的解决方案。
1.AccuSizer® A2000不溶性微粒检测仪如何成为25年药典合规检测方案的首选:
AccuSizer® A2000系列不溶性微粒检测仪符合中国药典CP<0903>、CP<3903>与美国药典USP<788>、USP<789> 等国际标准,内置ChP/USP/JP/EP/WHO等法规报告模板,符合FDA 21 CFR Part11 法规对数据完整性的要求,符合cGMP的管理规范。
AccuSizer® A2000系列不溶性微粒检测仪采用的原理是光阻法和光散射法技术融合,将传统光阻法2.0μm的检测下限下探至0.5μm,还支持模块化升级至A9000、搭载FX-Nano传感器,检测下限可进一步拓展至0.15μm,不仅满足当下的药典和各种规范要求,更能满足将来的行业趋势要求,提前适配各国药典法规对2μm以下微粒的检测预期。
除不溶性微粒检测外,AccuSizer® A2000系列不溶性微粒检测仪采用的SPOS技术,还适配2025年药典新增的0982第四法(传统光阻法不适用),可满足对乳剂、混悬剂等制剂的粒度分布检测需求。
2、AccuSizer® A2000不溶性微粒检测仪:
A2000系列仪器具备 1024 个数据通道及 32 个自定义通道,实现 0.01μm 精度的超高分辨率检测,灵敏度达10PPT等级,选配支持 50μL微量进样、自动进样(支持CETAC96孔板)、连续进样功能及自动稀释模块,兼容水相和有机相。传感器支持现场校准,无需返厂,模块化设计可灵活拓展功能。

AccuSizer® A2000USP
AccuSizer® A2000系列不溶性微粒检测仪具备仪器控制、数据采集、数理统计分析、出具报告以及权限管理、用户管理、数据安全性、审计追踪和电子签名等功能,完全符合FDA 21 CFR Part11法规对数据完整性的要求。可用于注射剂、眼用制剂、蛋白质注射液、药包材等场景的不溶性微粒检测。

参考文献
[1] 中华人民共和国药典(四部)<4206> 药包材不溶性微粒测定法[S]. 北京:中国医药科技出版社,2025.
[2] 包装材料不溶性微粒测定法:YBB 00272004-2015[S]. 国家药品监督管理局,2015.
[3] 中华人民共和国药典:通则<0903>不溶性微粒检查法[S]. 2025
[4] 中华人民共和国药典:<4206>药包材不溶性微粒测定法[S]. 2025..
[5] 国家药典委员会.2025年版《中国药典》实施有关事项解读(一)[EB/OL].(2025.03.26)[2025.11.04]. https://www.chp.org.cn/#/newsDetail?id=f4e637f3-b830-4a7c-a9c8-2a463c3e0677















